Les risques liés aux gaz : inflammable, toxique ou asphyxiant
L’air que nous respirons contient de l’oxygène et de l’azote, le gaz naturel ou méthane est utilisé dans de nombreux foyers pour le chauffage et la cuisine... Le gaz fait partie de notre environnement au quotidien mais si nous n’y prenons pas garde, cela peut s’avérer très vite dangereux.
Trois catégories de risques liés aux gaz existent :
- les risques d’incendie et/ou d’explosion liés à des gaz inflammables type méthane, butane, propane...
- le risque d’empoisonnement lié à des gaz toxiques type monoxyde de carbone (CO), hydrogène sulfuré (H₂S), dioxyde de carbone (CO₂), Chlore (Cl₂), ...
- les risques de suffocation ou asphyxie liés au manque d’oxygène, qui peut être consommé ou déplacé par un autre gaz.


Définition et les types de risques liés aux gaz
Par définition, un gaz est un essaim de molécules qui se déplacent aléatoirement et chaotiquement en rentrant en collision les unes avec les autres et avec ce qui les entourent. Les gaz remplissent tout volume disponible et, en raison de leur rapidité de déplacement, ils se mélangent rapidement dans toute l’atmosphère où ils sont introduits. Les gaz peuvent être plus lourds, plus légers ou de même densité que l’air. Certains sont odorants, d’autres inodores. Ils sont parfois colorés. Le fait de ne pas voir un gaz, de ne pas le sentir ou de ne pas le toucher ne signifie pas qu’il n’est pas là.
Le mot gaz vient du latin « chaos » qui désigne l’espace immense et ténébreux qui existait avant l’origine des choses dans la mythologie. Ce mot a été introduit au XVIIe siècle par le chimiste flamand Jean-Baptiste Van Helmont pour décrire une notion de vide.

Comprendre les risques liés aux gaz inflammables
Les composés d’hydrocarbures comme l'acétylène, l'ammoniac, l'hydrogène, le propane, le propylène, et le méthane sont tous des gaz inflammables. Ils sont également connus sous le nom de gaz combustibles.
La combustion est une réaction chimique dans laquelle l’oxygène se mélange rapidement à une autre substance entrainant un dégagement d’énergie, qui prend la forme de chaleur voir de flammes.
On peut représenter la combustion par le triangle du feu, trois facteurs qui doivent être réunis :
-
Une source ignition
-
Oxygène
-
Un combustible sous forme de gaz ou vapeur
C’est pour cela que dans tous systèmes de protection incendie, l’objectif est de supprimer l’un de ces éléments potentiellement dangereux.
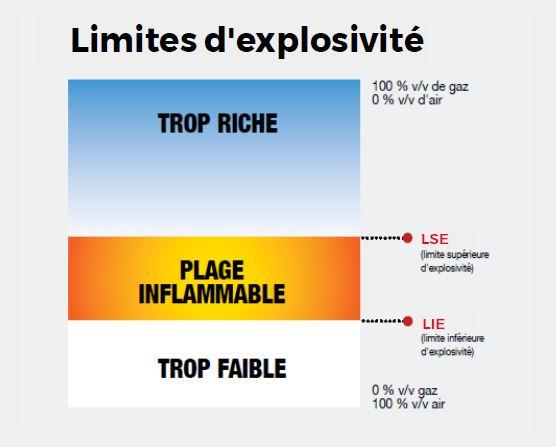
Les limites d’inflammabilité ou d’explosivité
Les limites d’inflammabilité ou d’explosivité d’un gaz correspondent aux concentrations limites du gaz dans l’air pour produire un mélange combustible (inflammation ou explosion) :
-
La limite minimale est appelée LIE (Limite Inférieur d’Explosivité)
-
La limite supérieure est appelée LSE (Limite Supérieure d’Explosivité)
En dessous de la LIE, on parle de mélange pauvre car le gaz est en quantité insuffisante pour produire une explosion. Le risque incendie croît à mesure que le pourcentage de gaz inflammable augmente. Au-delà de la LES, le mélange manque d’oxygène. L’air devient trop riche pour brûler, réduisant ainsi les chances d’allumage. En règle générale, une augmentation de la pression, de la température ou de la concentration augmente la plage d’inflammabilité.
Dans un contexte classique, les installations industrielles ne présentent pas de fuite de gaz ou seulement à l’état de trace. Les détecteurs de gaz sont chargés de surveiller les risques avant la combustion, c’est-à-dire de mesurer les concentrations de gaz compris entre 0% et la limite inférieure d’explosivité (LIE). Lorsque la limite inférieure est atteinte, des procédures de coupure ou d’évacuation du site sont lancées. En pratique, ces mesures sont plutôt prises à des concentrations inférieures à 50% de la valeur LIE afin de disposer d’une marge de sécurité suffisante.
Dans le cas des espaces confinés (environnement clos ou non ventilés), une concentration supérieure à la LES peut parfois survenir. Le danger réside à l’ouverture des portes et des écoutilles car l’entrée d’air provenant de l’extérieur peut diluer les gaz pour former un mélange combustible dangereux. De ce fait, certains gaz sont parfumés afin de faciliter la détection de fuites.
Le point d’inflammation
A partir d’une certaine température, les gaz inflammables s’enflamment même sans étincelle ou flamme. On appelle cette température le point d’inflammation. La température de surface des appareils utilisés en zone dangereuse ne doit pas dépasser le point d’inflammation. Une température de surface maximale est donc indiquée sur les appareils.
Le point d’éclair (point congélation en °C)
Il s’agit de la température la plus basse à laquelle la surface du liquide produit des vapeurs suffisantes pour allumer une petite flamme.
Densité de vapeur
Elle aide à déterminer l’emplacement du capteur. La densité de gaz/vapeur est comparée à l’air : lorsque l’air = 1,0 alors Densité de vapeur < 1 augmente et Densité de vapeur > 1 chute.
Comprendre les risques liés aux gaz toxiques
Les gaz inflammables et les gaz toxiques sont traités séparément car ils impliquent des risques, des réglementations et des capteurs différents. Cependant, il existe de nombreux gaz qui sont à la fois combustibles et toxiques, ce qui implique d’homologuer les détecteurs de gaz toxiques pour les zones dangereuses.
Dans le cas des substances toxiques, la principale préoccupation - hormis les problèmes environnementaux - est l’effet de ces gaz sur les employés. Une inhalation, une ingestion ou une pénétration par la peau peuvent être nocifs même à de très faibles concentrations. Le nombre de décès par exposition à des gaz toxiques est supérieur à celui des décès par explosions dues à des gaz inflammables.
Les mesures les plus utilisées pour la concentration de gaz toxiques sont les parties par million (ppm) et les parties par milliard (ppb). Par exemple, 1 ppm correspond à une pièce remplie d’un million de balles parmi lesquelles se trouve 1 balle rouge : La balle rouge représente 1 ppm. Cependant, il est essentiel de mesurer le temps d’exposition et pas seulement la concentration des gaz car les effets nocifs résultent souvent d’expositions régulières sur le long terme.
Les VLEPs
Une notion importante est le terme de « Valeurs Limites d’Exposition Professionnel » ou VLEP. Le but d’une VLEP est d’empêcher l’apparition d’une atteinte à la santé de manière irréversible lié à l’utilisation d’une ou plusieurs substances dangereuses. Elle protège des effets sur la santé mais pas les risques d’explosion. En d’autres termes, le but est de s’assurer que les niveaux d’exposition sur le lieu de travail sont inférieurs aux limites légales. Ces limites sont un outil précieux en matière d’évaluation et de gestion des risques.
Pour obtenir une mesure représentative du niveau de contamination de l’air inhalé, trois éléments sont nécessaires :
-
une étude de terrain (profil des expositions potentielles)
-
une surveillance personnelle grâce à des détecteurs portés par les utilisateurs
-
un prélèvement qui s’effectue le plus près possible de la zone de respiration.
La toxicité du gaz concerné doit absolument être prise en compte. Par exemple, un détecteur qui mesure uniquement une moyenne pondérée ou un détecteur qui réalise un prélèvement pour une analyse en laboratoire ne protège pas un employé contre une courte exposition à une dose mortelle d’une substance extrêmement toxique. Toutefois, il peut être normal de dépasser temporairement les niveaux limites d’exposition à long terme dans certaines parties d’une usine sans nécessairement déclencher une situation d’alerte. Le détecteur optimal doit donc permettre de surveiller les niveaux d’exposition à long terme et à court terme, ainsi que les niveaux d’alarme instantanés.
Les temps d’exposition sont estimés sur huit heures (VLEP-8h) et 15 minutes (VLCT). Pour certaines substances, une brève exposition est si critique qu’elles n’ont qu’une limite d’exposition à court terme, qui ne doit jamais être dépassée, même très brièvement. La cancérogénicité, les effets toxiques sur la reproduction, l’irritation et la sensibilisation sont pris en compte lors de l’élaboration d’une proposition pour une VLEP selon les connaissances scientifiques actuelles.

Comprendre les risques liés à l’oxygène
Dans le cas du manque d’oxygène (ou asphyxie)
Nous avons tous besoin de respirer l’oxygène (O₂) contenu dans l’air pour vivre. L’oxygène n’est toutefois que l’un des nombreux gaz présents dans l’air. Dans l’air ambiant ordinaire, sa concentration est de 20,9 % v/v. Lorsque ce taux chute en deçà de 19,5 %, l’air est considéré comme appauvri en oxygène. A moins de 16% v/v, l’air est dangereux pour l’être humain.
L’appauvrissement en oxygène a plusieurs origines :
-
un déplacement
-
une combustion
-
une réaction chimique
-
une action bactérienne
Dans le cas d’enrichissement en oxygène
Le danger lié à un air trop riche en oxygène est également souvent oublié. L’augmentation du taux d’O₂ accroit l’inflammabilité des matériaux et des gaz. Au-delà de 24%, des combustions spontanées peuvent survenir, notamment des vêtements.
Le soudage oxyacétylénique combine l’oxygène et l’acétylène gazeux pour produire des températures extrêmement élevées. Les atmosphères enrichies en oxygène peuvent représenter un danger dans d’autres environnements, par exemple les zones de fabrication ou d’entreposage de système de propulsion par réaction et de produits de blanchiment de l’industrie du papier ou les usines de traitement des eaux.
Les capteurs doivent être spécifiquement certifiés pour une utilisation en atmosphères enrichies en O₂.
Découvrez nos gammes pour la détection de gaz

Détection de gaz portable

Détection de gaz fixe




